Lo que la literatura científica y los organismos sanitarios han documentado sobre el vapeo de cannabidiol desde el brote EVALI de 2019
La literatura indexada en PubMed sobre cigarrillos electrónicos y cannabinoides ha crecido de manera acelerada desde el verano de 2019, cuando los Centros para el Control y la Prevención de Enfermedades de Estados Unidos registraron el primer brote sanitario asociado al uso de dispositivos de vaporización. Este artículo, preparado por el equipo editorial de Justbob, recopila lo que han publicado las agencias reguladoras y las revistas peer-reviewed sobre el vapeo de cannabidiol, sus riesgos documentados y el marco regulatorio que lo rodea en Europa y en España.
El propósito del texto es estrictamente documental. No encontrará usted aquí instrucciones de uso, indicaciones de consumo ni recomendaciones sobre dispositivos, líquidos o concentraciones. Lo que encontrará es un recorrido por la evidencia epidemiológica publicada, por los pronunciamientos de la FDA, de la OMS y de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), y por las advertencias que la comunidad neumológica internacional ha emitido sobre la categoría cigarrillo electrónico CBD.
El brote EVALI de 2019: el inicio de la vigilancia epidemiológica sobre los dispositivos de vaporización
El acrónimo EVALI, acuñado por los CDC en 2019, designa la e-cigarette or vaping product use-associated lung injury. Entre agosto de 2019 y febrero de 2020 se notificaron 2.807 hospitalizaciones y 68 muertes confirmadas en Estados Unidos, según los informes de vigilancia publicados por los CDC. La edad media de los pacientes era de 24 años y el 95 % presentaba síntomas respiratorios agudos que requerían hospitalización.
Lea también: Los terpenos del cannabis: qué son y cómo interpretar su perfil aromático
La investigación clínica publicada por Blount y colaboradores en The New England Journal of Medicine (2020) identificó el acetato de vitamina E como agente etiológico primario. Los autores analizaron muestras de líquido broncoalveolar de 51 pacientes afectados por EVALI: en 48 de ellos se detectó acetato de vitamina E, un aditivo utilizado por el mercado no regulado para diluir extractos cannábicos en líquidos de CBD y de THC.
El hallazgo cambió la percepción pública sobre el vapeo de cannabinoides. La FDA emitió en noviembre de 2019 una advertencia sanitaria formal en la que recomendaba a la población evitar los productos de vaporización que contuvieran THC o aditivos añadidos, especialmente los adquiridos en canales no regulados. Los CDC mantuvieron la vigilancia hasta 2020 y clasificaron el EVALI como emergencia de salud pública.
El acetato de vitamina E y los riesgos documentados en los aerosoles cannabinoides
El acetato de vitamina E, denominado químicamente tocoferol acetato, se utiliza en la industria cosmética como antioxidante. En el mercado no regulado de líquidos de CBD comenzó a añadirse hacia 2018 como diluyente barato de extractos concentrados, con el objetivo de aumentar la viscosidad y el volumen del producto sin modificar su aspecto visual.
El problema, según la investigación publicada en Chemical Research in Toxicology (2020), es que el tocoferol acetato, al calentarse por encima de los 200 °C dentro de un cigarrillo electrónico, se descompone en cetena, un compuesto químicamente similar al fosgeno que provoca daño alveolar agudo. La cetena es la molécula que las autopsias EVALI identificaron como responsable del cuadro clínico.
Los riesgos documentados del vapeo con líquidos no regulados, según la revisión sistemática publicada por Gravely y colaboradores (2020), pueden resumirse en la tabla siguiente. Ofrecemos a usted una síntesis crítica de los hallazgos, no una recomendación de uso.
| Riesgo documentado | Mecanismo | Referencia |
|---|---|---|
| Lesión pulmonar aguda (EVALI) | Descomposición térmica del acetato de vitamina E en cetena a 200 °C, con daño alveolar bilateral y necesidad de soporte ventilatorio | Blount et al., NEJM 2020 |
| Neumonía lipoidea exógena | Acumulación de lípidos del vehículo del líquido (MCT, propilenglicol, glicerina vegetal) en los alvéolos pulmonares | Gravely et al., 2020 |
| Broncoespasmo agudo | Reacciones inmediatas de vías respiratorias en usuarios sensibles a aromas sintéticos y diluyentes | CDC vigilancia 2019-2020 |
| Contaminación por metales pesados | Níquel, plomo y cromo liberados por resistencias de baja calidad tras ciclos repetidos de calentamiento | Olmedo et al., Environ Health Perspect 2018 |
| Pesticidas residuales | Myclobutanil y otros compuestos hallados en productos CBD no sometidos a análisis de laboratorio independiente | CDC alerta 2019 |
| Aditivos aromatizantes | Diacetil y 2,3-pentanediona vinculados a bronquiolitis obliterante, detectados en aromas saborizantes de líquidos no regulados | Allen et al., Environ Health Perspect 2016 |
Esta síntesis procede de metaanálisis y alertas oficiales. La literatura subraya, sin margen de interpretación, que el mercado no regulado concentra el grueso de los riesgos. Los productos adquiridos a proveedores sin trazabilidad analítica son, estadísticamente, los implicados en las hospitalizaciones EVALI.


Farmacocinética del cannabidiol inhalado: lo que ha publicado la investigación peer-reviewed
La farmacocinética del cannabidiol por vía respiratoria ha sido objeto de varias publicaciones científicas. El trabajo de Millar y colaboradores en Frontiers in Pharmacology (2018) sistematizó la biodisponibilidad del cannabidiol por distintas vías de administración en contextos de investigación clínica controlada, no de consumo recreativo.
Los autores describieron que, en los ensayos clínicos autorizados por las agencias reguladoras, la vía inhalatoria presenta una biodisponibilidad estimada entre el 11 % y el 45 %, con gran variabilidad interindividual. Los picos plasmáticos se alcanzan en 3 a 10 minutos, frente a las 1 a 2 horas de la vía oral. Sin embargo, los autores subrayan que estos datos proceden de preparaciones farmacéuticas estandarizadas, no de cbd vape adquirido en canales comerciales.
La diferencia es esencial desde el punto de vista analítico. Los preparados utilizados en los ensayos clínicos son productos con estandarización regulatoria, trazabilidad completa y control analítico por la EMA o la FDA. Los líquidos comercializados bajo la etiqueta cigarrillo electrónico CBD en el mercado europeo, salvo raras excepciones farmacéuticas, no están sometidos a ese nivel de escrutinio.
Lea también: Perfil terpénico del cannabis: qué es y cómo interpretarlo
Datos epidemiológicos posteriores a 2020: qué ha aportado la vigilancia europea
Tras la crisis EVALI, las autoridades sanitarias europeas reforzaron los mecanismos de vigilancia. El Centro Europeo para la Prevención y el Control de Enfermedades (ECDC) incorporó los aerosoles cannabinoides a su listado de sustancias bajo seguimiento activo. Entre 2020 y 2024, ningún país europeo ha registrado brotes de magnitud comparable al EVALI, aunque se han notificado casos aislados en Alemania, Francia y Países Bajos asociados a líquidos adquiridos en canales sin autorización.
Las diferencias entre los dos mercados no son casuales. El mercado norteamericano de 2019 era dominado por THC y por proveedores sin licencia estatal. El mercado europeo de líquido de CBD ha crecido en paralelo con una regulación más estricta en varios países, lo que ha limitado la aparición de productos adulterados con acetato de vitamina E. Sin embargo, las agencias europeas advierten que la compra en línea sin verificación de origen sigue expuesta a los mismos riesgos identificados por los CDC.
Una revisión publicada en European Respiratory Journal en 2022 analizó 147 casos europeos de lesión pulmonar asociada al vapeo entre 2019 y 2021. Los autores identificaron tres patrones recurrentes: aditivos lipídicos en el vehículo, aromas saborizantes industriales y contaminantes procedentes de dispositivos no homologados. La recomendación clínica fue clara: la ausencia de estándares analíticos armonizados en Europa impide ofrecer al público garantías equiparables a las de un medicamento registrado.
Debe usted considerar que estos datos proceden exclusivamente de productos comercializados como líquidos para cigarrillo electrónico, no de los derivados de cáñamo industrial vendidos con finalidades técnicas y ornamentales, que pertenecen a una categoría regulatoria distinta.
Pronunciamientos de la OMS y de la Organización Mundial de la Salud sobre el cannabidiol
El informe ECDD de 2018 sobre cannabidiol, elaborado por el Comité de Expertos en Farmacodependencia de la Organización Mundial de la Salud, concluyó que el cannabidiol puro no induce efectos de dependencia ni justifica su inclusión en los listados de sustancias fiscalizadas internacionales. El documento se refiere específicamente al cannabidiol como molécula, no a formulaciones concretas ni a vías de administración específicas.
La OMS no se pronuncia en ese informe sobre la seguridad del vapeo de cannabidiol. El documento aclara que cualquier preparación comercial debe evaluarse individualmente en función de sus excipientes, su método de producción y su marco regulatorio nacional. El cannabidiol de grado farmacéutico, utilizado en medicamentos aprobados como Epidyolex, se administra por vía oral, no inhalatoria.
Los pronunciamientos posteriores de agencias nacionales han seguido la misma línea. La autoridad sanitaria del Reino Unido (MHRA), la Comisión Federal Suiza y la FDA estadounidense han emitido entre 2019 y 2023 advertencias sobre la falta de ensayos clínicos controlados que respalden el uso inhalatorio de cannabidiol fuera de contextos de investigación.
Marco regulatorio del cigarrillo electrónico CBD en España y en la Unión Europea
En la Unión Europea, la Directiva 2014/40/UE sobre Productos del Tabaco establece los requisitos técnicos para los cigarrillos electrónicos con nicotina: potencia máxima, capacidad de depósito, composición del líquido, notificación previa a la comercialización. La directiva no incluye disposiciones específicas para los líquidos de CBD, que han quedado en un vacío regulatorio interpretado de manera distinta por cada Estado miembro.
En España, la AEMPS considera los líquidos de cannabidiol destinados a vaporización como productos no autorizados salvo que hayan obtenido una evaluación específica como medicamento o como novel food. El Ministerio de Sanidad ha emitido varias circulares recordando que la venta de líquidos CBD para cigarrillo electrónico como productos de consumo humano carece de cobertura legal armonizada.
Los productos de aceite de CBD, de marihuana CBD, de hachís CBD y de extractos de CBD comercializados por Justbob pertenecen a una categoría regulatoria distinta: derivados de cáñamo industrial (Cannabis sativa L. inscrito en el Catálogo Común Europeo), con THC inferior al 0,2 %, destinados a uso técnico, científico, ornamental y de perfumación de ambientes.
La voz de la neumología española: Dr. Alfonso Moreno Castillo sobre los riesgos documentados del vapeo
El Dr. Alfonso Moreno Castillo, neumólogo del Hospital Universitario La Paz de Madrid y miembro del grupo de trabajo sobre tabaquismo y dispositivos electrónicos de la Sociedad Española de Neumología y Cirugía Torácica, ha publicado varios análisis sobre el impacto clínico de los cigarrillos electrónicos desde 2019.
En una entrevista publicada en Revista Española de Salud Pública en 2022, el Dr. Moreno Castillo sintetizó así el estado de la cuestión: “La comunidad neumológica internacional ha acumulado, desde el brote EVALI de 2019, evidencia suficiente para afirmar que el vapeo no es una práctica inocua. La inhalación de aerosoles cannabinoides con vehículos lipídicos o con diluyentes sintéticos genera riesgos documentados sobre el parénquima pulmonar. Los estudios peer-reviewed no permiten hoy respaldar la seguridad del cannabidiol por vía inhalatoria fuera de los contextos farmacéuticos estandarizados”.
La posición del investigador es clara respecto a la comunicación pública: los productos derivados de cáñamo industrial deben describirse con precisión regulatoria, sin asimilarlos a las categorías farmacéuticas ni a las vías de administración no autorizadas. El marketing que presenta los productos CBD como alternativas de vapeo está, según Moreno Castillo, en contradicción directa con los pronunciamientos de la FDA, de la OMS y de las sociedades científicas europeas.
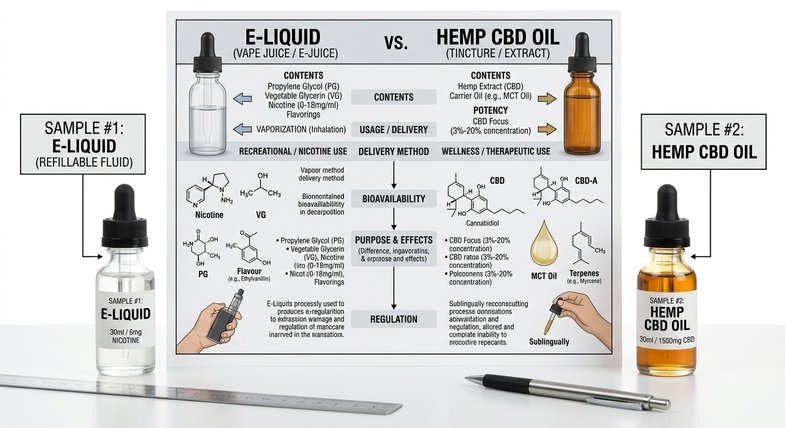

Por qué la literatura científica distingue entre cannabidiol farmacéutico y líquidos CBD comerciales
La literatura peer-reviewed distingue tres categorías claramente diferenciadas cuando habla de cannabidiol:
- Cannabidiol farmacéutico: principio activo estandarizado utilizado en medicamentos aprobados por la EMA y la FDA (Epidyolex/Epidiolex). Se administra por vía oral, no inhalatoria. Sujeto a farmacovigilancia y ensayos clínicos controlados.
- Cannabidiol de investigación: preparaciones utilizadas en protocolos de investigación académica con registro ético y trazabilidad analítica completa.
- Cáñamo industrial con cannabidiol: derivado vegetal de variedades de Cannabis sativa L. inscritas en el Catálogo Común Europeo, con THC inferior al 0,2 %. Destinado a uso técnico, científico, ornamental y de perfumación.
Confundir estas tres categorías es el error más frecuente en la comunicación pública sobre cannabidiol. La literatura académica siempre especifica la categoría del producto analizado antes de presentar resultados. Los textos divulgativos que mezclan las tres categorías generan expectativas incorrectas sobre los productos comerciales.
Aclaración sobre los productos Justbob y el vapeo
Los productos comercializados por Justbob no son adecuados para combustión ni para vaporización. Se trata de derivados de cáñamo industrial (Cannabis sativa L. inscrito en el Catálogo Común Europeo), con THC inferior al 0,2 %, analizado diariamente en laboratorio. Están destinados a finalidades técnicas, científicas, ornamentales, de coleccionismo y de perfumación de ambientes.
Justbob no comercializa líquidos para cigarrillo electrónico, ni dispositivos de vaporización, ni cartuchos, ni productos de ningún tipo destinados al consumo humano. Los textos del blog sobre literatura científica del vapeo de cannabinoides tienen carácter informativo-documental y en ningún caso constituyen una guía de uso ni un respaldo al vapeo fuera de los contextos farmacéuticos regulados.
Los productos de Justbob no son medicamentos, ni alimentos, ni complementos alimenticios, ni cosméticos. No diagnostican, no tratan, ni curan enfermedad alguna. Para cualquier cuestión relacionada con la salud, consulte a un profesional sanitario colegiado.
¿Desea explorar el catálogo de productos derivados del cáñamo industrial disponibles en el portal? Visite la tienda online de Justbob y consulte los certificados de análisis por lote de cada categoría.
Preguntas frecuentes sobre la literatura científica del vapeo de cannabidiol
¿Qué es EVALI y por qué cambió la percepción del vapeo?
EVALI es el acrónimo acuñado por los CDC de Estados Unidos en 2019 para describir un síndrome pulmonar agudo asociado al uso de cigarrillos electrónicos. Entre agosto de 2019 y febrero de 2020 se registraron 2.807 hospitalizaciones y 68 muertes confirmadas. El estudio publicado por Blount y colaboradores en The New England Journal of Medicine (2020) identificó el acetato de vitamina E como agente etiológico en 48 de 51 casos analizados.
¿La FDA considera seguros los líquidos de CBD para cigarrillo electrónico?
La FDA ha emitido desde 2019 varias advertencias sobre el vapeo de productos cannabinoides adquiridos en canales no regulados. La agencia no ha aprobado ningún líquido CBD para cigarrillo electrónico como producto seguro para el consumo humano. El único medicamento a base de cannabidiol aprobado por la FDA es Epidyolex, que se administra por vía oral, no inhalatoria.
¿Qué dice la OMS sobre el vapeo de cannabidiol?
El informe ECDD 2018 de la OMS sobre cannabidiol se pronuncia sobre la molécula, no sobre vías de administración específicas. La Organización aclara que cada preparación comercial debe evaluarse individualmente en función de sus excipientes y su marco regulatorio. No existe un pronunciamiento oficial de la OMS que respalde la seguridad del vapeo de cannabidiol fuera de contextos farmacéuticos estandarizados.
¿Los productos de Justbob son aptos para vapeo o combustión?
No. Los productos de Justbob son derivados de cáñamo industrial (Cannabis sativa L.), con THC inferior al 0,2 %, comercializados para uso técnico, científico, ornamental, de coleccionismo y de perfumación de ambientes. No son adecuados para combustión ni para vaporización, ni están destinados al consumo humano en ninguna forma. Justbob no comercializa líquidos para cigarrillo electrónico ni dispositivos de vaporización.